Явление превращения вещества из жидкого состояния в газообразное называется парообразованием . Парообразование может осуществляться в виде двух процессов: и.
Второй процесс парообразования - кипение. Наблюдать этот процесс можно с помощью простого опыта, нагревая воду в стеклянной колбе. При нагревании воды в ней через некоторое время появляются пузырьки, в которых содержатся воздух и насыщенный водяной пар, который образуется при испарении воды внутри пузырьков. При повышении температуры давление внутри пузырьков растёт, и под действием выталкивающей силы они поднимаются вверх. Однако, поскольку температура верхних слоёв воды меньше, чем нижних, пар в пузырьках начинает конденсироваться, и они сжимаются. Когда вода прогреется по всему объёму, пузырьки с паром поднимаются до поверхности, лопаются, и пар выходит наружу. Вода кипит. Это происходит при такой температуре, при которой давление насыщенного пара в пузырьках равно атмосферному давлению.
Процесс парообразования, происходящий во всем объёме жидкости при определённой температуре, называют . Температуру, при которой жидкость кипит, называют температурой кипения .
Эта температура зависит от атмосферного давления. При повышении атмосферного давления температура кипения возрастает.
Опыт показывает, что в процессе кипения температура жидкости не изменяется, несмотря на то, что извне поступает энергия. Переход жидкости в газообразное состояние при температуре кипения связан с увеличением расстояния между молекулами и соответственно с преодолением притяжения между ними. На совершение работы по преодолению сил притяжения расходуется подводимая к жидкости энергия. Так происходит до тех пор, пока вся жидкость не превратится в пар. Поскольку жидкость и пар в процессе кипения имеют одинаковую температуру, то средняя кинетическая энергия молекул не изменяется, увеличивается лишь их потенциальная энергия.
На рисунке приведён график зависимости температуры воды от времени в процессе её нагревания от комнатной температуры до температуры кипения (АВ), кипения (ВС), нагревания пара (CD), охлаждения пара (DE), конденсации (EF) и последующего охлаждения (FG).
Для превращения разных веществ из жидкого состояния в газообразное требуется разная энергия, эта энергия характеризуется величиной, называемой удельной теплотой парообразования.
Удельная теплота парообразования (L ) — это величина, равная отношению количества теплоты, которое нужно сообщить веществу массой 1 кг, для превращения его из жидкого состояния в газообразное при температуре кипения.
Единица удельной теплоты парообразования - [L ] = Дж/кг.
Чтобы рассчитать количество теплоты Q, которое необходимо сообщить веществу массой тп для его превращения из жидкого состояния в газообразное, необходимо удельную теплоту парообразования (L ) умножить на массу вещества: Q = Lm.
При конденсации пара выделяется некоторое количество теплоты, причем его значение равно значению количества теплоты, которое необходимо затратить для превращения жидкости в пар при той же температуре.
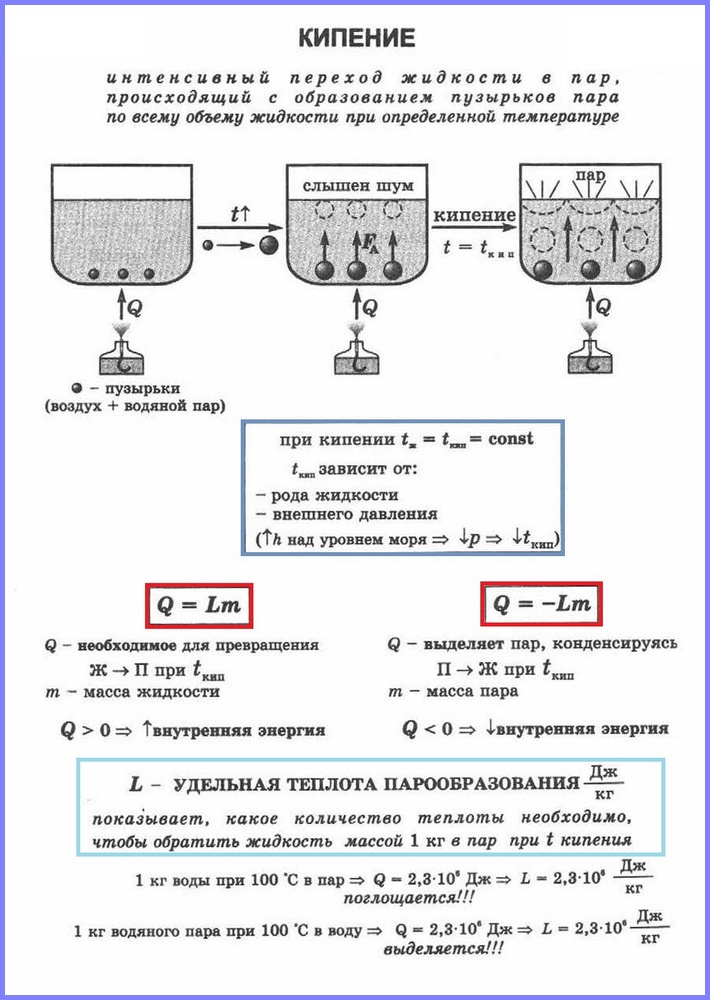
Кипение, как мы видели, тоже испарение, только сопровождается оно быстрым образованием и ростом пузырьков пара. Очевидно, что во время кипения необходимо подводить к жидкости определённое количество теплоты. Это количество теплоты идёт на образование пара. Причём различные жидкости одной и той же массы требуют разное количество теплоты для обращения их в пар при температуре кипения.
Опытами было установлено, что для испарения воды массой 1 кг при температуре 100 °С требуется 2,3 10 6 Дж энергии. Для испарения эфира массой 1 кг, взятого при температуре 35 °С, необходимо 0,4 10 6 Дж энергии.
Следовательно, чтобы температура испаряющейся жидкости не изменялась, к жидкости необходимо подводить определённое количество теплоты.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой L. Её единица - 1 Дж/кг.
Опытами установлено, что удельная теплота парообразования воды при 100 °С равна 2,3 10 6 Дж/кг. Иными словами, для превращения воды массой 1 кг в пар при температуре 100 °С требуется 2,3 10 6 Дж энергии. Следовательно, при температуре кипения внутренняя энергия вещества в парообразном состоянии больше внутренней энергии такой же массы вещества в жидком состоянии.
Таблица 6.
Удельная теплота парообразования некоторых веществ (при температуре кипения и нормальном атмосферном давлении)
Соприкасаясь с холодным предметом, водяной пар конденсируется (рис. 25). При этом выделяется энергия, поглощённая при образовании пара. Точные опыты показывают, что, конденсируясь, пар отдаёт то количество энергии, которое пошло на его образование.

Рис. 25. Конденсация пара
Следовательно, при превращении 1 кг водяного пара при температуре 100 °С в воду той же температуры выделяется 2,3 10 6 Дж энергии. Как видно из сравнения с другими веществами (табл. 6), эта энергия довольно велика.
Освобождающаяся при конденсации пара энергия может быть использована. На крупных тепловых электростанциях отработавшим в турбинах паром нагревают воду.
Нагретую таким образом воду используют для отопления зданий, в банях, прачечных и для других бытовых нужд.
Чтобы вычислить количество теплоты Q, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования L умножить на массу m:
Из этой формулы можно определить, что
m = Q / L, L = Q / m
Количество теплоты, которое выделяет пар массой т, конденсируясь при температуре кипения, определяется по той же формуле.
Пример . Какое количество энергии требуется для превращения воды массой 2 кг, взятой при температуре 20 °С, в пар? Запишем условие задачи и решим её.

Кипение - это интенсивное парообразование, которое происходит при нагревании жидкости не только с поверхности, но и внутри неё.
Кипение происходит с поглощением теплоты.
Большая часть подводимой теплоты расходуется на разрыв связей между частицами вещества, остальная часть - на работу, совершаемую при расширении пара.
В результате энергия взаимодействия между частицами пара становится больше, чем между частицами жидкости, поэтому внутренняя энергия пара больше, чем внутренняя энергия жидкости при той же температуре.
Количество теплоты, необходимое для перевода жидкости в пар в процессе кипения можно расчитать по формуле:

где m - масса жидкости (кг),
L - удельная теплота парообразования.
Удельная теплота парообразования показывает, какое количество теплоты необходимо, чтобы превратитъ в пар 1 кг данного вещества при температуре кипения.
Единица удельной теплоты парообразования в системе СИ:
[ L ] = 1 Дж/ кг
С ростом давления температура кипения жидкости повышается, а удельная теплота парообразования уменьшается и наоборот.

Во время кипения температура жидкости не меняется.
Температура кипения зависит от давления, оказываемого на жидкость.
Каждое вещество при одном и том же давлении имеет свою температуру кипения.
С увеличением атмосферного давления кипение начинается при более высокой температуре, при уменьшении давления - наоборот..
Так, например, вода кипит при 100 °С лишь при нормальном атмосферном давлении.
ЧТО ЖЕ ПРОИСХОДИТ ВНУТРИ ЖИДКОСТИ ПРИ КИПЕНИИ?

Кипение представляет собой переход жидкости в пар с непрерывным образованием и ростом в жидкости пузырьков пара, внутрь которых происходит испарение жидкости. В начале нагревания вода насыщена воздухом и имеет комнатную температуру. При нагревании воды, растворенный в ней газ выделяется на дне и стенках сосуда, образуя воздушные пузырьки. Они начинают появляться задолго до кипения. В эти пузырьки испаряется вода. Пузырек, наполненный паром, при достаточно высокой температуре начинает раздуваться.

Достигнув определенных размеров он отрывается от дна, поднимается к поверхности воды и лопается. При этом пар покидает жидкость. Если вода прогрета недостаточно, то пузырек пара, поднимаясь в холодные слои, схлопывается. Возникающие при этом колебания воды приводят к появлению во всем объеме воды огромного количества мелких пузырьков воздуха: так называемый "белый ключ".

На воздушный пузырек объемом на дне сосуда действует подъемная сила:
Fпод = Fархимеда - Fтяжести
Пузырек прижат ко дну, поскольку на нижнюю поверхность силы давления не действуют. При нагреве пузырек увеличивается за счет выделения в него газа и отрывается от дна, когда подъемная сила будет немного больше прижимающей. Размер пузырька, способного оторваться от дна, зависит от его формы. Форма пузырьков на дне определяется смачиваемостью дна сосуда.
Неоднородность смачивания и слияние пузырьков на дне приводили к увеличению их размеров. При больших размерах пузырька при подъеме сзади него образуются пустоты, разрывы и завихрения.
Когда пузырек лопается, вся окружающая его жидкость устремляется внутрь, и возникает кольцевая волна. Смыкаясь, она выбрасывает вверх столбик воды.

При схлопывании лопающихся пузырьков в жидкости распространяются ударные волны ультразвуковых частот, сопровождаемые слышимым шумом. Для начальных стадий кипения характерны самые громкие и высокие звуки (на стадии "белого ключа" чайник "поет").
(источник: virlib.eunnet.net)
ТЕМПЕРАТУРНЫЙ ГРАФИК ИЗМЕНЕНИЯ АГРЕГАТНЫХ СОСТОЯНИЙ ВОДЫ

ЗАГЛЯНИ НА КНИЖНУЮ ПОЛКУ!
ИНТЕРЕСНО
Зачем в крышке чайника делают дырочку?
Для выхода пара. Без дырочки в крышке пар может выплеснуть воду через носик чайника.
___
Продолжительность варки картофеля, начиная с момента кипения, не зависит от мощности нагревателя. Продолжительность определяется временем пребывания продукта при температуре кипения.
Мощность нагревателя не влияет на температуру кипения, а влияет только на скорость испарения воды.
Кипением можнозаставить воду замерзнуть. Для этого надо производить откачку воздуха и водяного пара из сосуда, где находится вода, так, чтобы вода все время кипела.
«Горшки легко закипают через край – к ненастью!»
Падение атмосферного давления, сопровождающее ухудшение погоды, является причиной того, что молоко быстрее «убегает».
___
Очень горячий кипяток можно получить на дне глубоких шахт, где давление воздуха значительно больше, чем на поверхности Земли. Так на глубине 300 м вода закипит при 101 ͦ С. При давлении воздуха в 14 атмосфер вода закипает при 200 ͦ С.
Под колоколом воздушного насоса можно получить «кипяток» при 20 ͦ С.
На Марсе мы пили бы «кипяток» при 45 ͦ С.
Соленая вода кипит при температуре выше 100 ͦ C.
___
В горных районах на значительной высоте при пониженном атмосферном давлении вода кипит при температурах ниже, чем 100 ͦ Цельсия.

Ждать, пока сварится такой обед, приходится дольше.
Польем холодненькой… и закипит!
Обычно вода кипит при 100 градусах Цельсия. Нагреем воду в колбе на горелке до кипения. Погасим горелку. Вода перестает кипеть. Закроем колбу пробкой и начнем осторожно лить на пробку струйкой холодную воду. Каково? Вода опять закипела!
..............................Под струей холодной воды водичка в колбе, а вместе с ней и водяные пары начинают остывать.
Объем паров уменьшается, и давление над поверхностью воды меняется...
А как ты думаешь, в какую сторону?
... Температура кипения воды при пониженном давлении меньше 100 градусов, и вода в колбе вскипает вновь!
____
При приготовлении пищи давление внутри кастрюли - "скороварки" - около 200 кПа, и суп в такой кастрюле сварится значительно быстрее.
Можно набрать в шприц воду примерно до половины, закрыть той же пробочкой и резко потянуть за поршень. В воде возникнет масса пузырьков, говорящих, что начался процесс кипения воды (и это при комнатной температуре!).
___
При переходе вещества в газообразное состояние его плотность уменьшается примерно в 1000 раз.
___
У первых электрочайников нагреватели находились под донышком. Вода не вступала в контакт с нагревателем и закипала очень долго. В 1923 году Артур Лардж сделал открытие: он поместил нагреватель в особую медную трубку и поместил её внутрь чайника. Вода быстро закипала.
В США разработаны самоохлаждающиеся банки для прохладительных напитков. В банку вмонтирован отсек с легкокипящей жидкостью. Если в жаркий день раздавить капсулу, жидкость начнет бурно кипеть, отнимая тепло у содержимого банки, и за 90 секунд температура напитка понижается на 20–25 градусов Цельсия.
НУ, ПОЧЕМУ ЖЕ?
А как ты думаешь, можно ли сварить яйцо вкрутую, если вода закипает при температуре ниже, чем 100 градусов Цельсия?
____
Будет ли кипеть вода в кастрюле, которая плавает в другой кастрюле с кипящей водой?
Почему?
___
Можно ли заставить кипеть воду, не нагревая ее?

На этом уроке мы уделим внимание такому виду парообразования, как кипение, обсудим его отличия от рассмотренного ранее процесса испарения, введем такую величину, как температура кипения, и обсудим, от чего она зависит. В конце урока введем очень важную величину, описывающую процесс парообразования - удельную теплоту парообразования и конденсации.
Тема: Агрегатные состояния вещества
Урок: Кипение. Удельная теплота парообразования и конденсации
На прошлом уроке мы уже рассмотрели один из видов парообразования - испарение - и выделили свойства этого процесса. Сегодня мы обсудим такой вид парообразования, как процесс кипения, и введем величину, которая численно характеризует процесс парообразования - удельная теплота парообразования и конденсации.
Определение. Кипение (рис. 1) - это процесс интенсивного перехода жидкости в газообразное состояние, сопровождающийся образованием пузырьков пара и происходящий по всему объему жидкости при определенной температуре, которую называют температурой кипения.
Сравним два вида парообразования между собой. Процесс кипения более интенсивен, чем процесс испарения. Кроме того, как мы помним, процесс испарения протекает при любой температуре выше температуры плавления, а процесс кипения - строго при определенной температуре, которая является различной для каждого из веществ и называется температурой кипения. Еще следует отметить, что испарение происходит только со свободной поверхности жидкости, т. е. с области, разграничивающей ее с окружающими газами, а кипение - сразу со всего объема.
Более подробно рассмотрим протекание процесса кипения. Представим ситуацию, с которой многие из нас неоднократно сталкивались, - это нагревание и кипячение воды в некотором сосуде, например, в кастрюле. В ходе нагревания воде будет передаваться определенное количество теплоты, что будет приводить к увеличению ее внутренней энергии и увеличению активности движения молекул. Этот процесс будет протекать до определенного этапа, пока энергия движения молекул не станет достаточной для начала кипения.
В воде присутствуют растворенные газы (или другие примеси), которые выделяются в ее структуре, что приводит к так называемому возникновению центров парообразования. Т. е. именно в этих центрах начинает происходить выделение пара, и по всему объему воды образовываются пузырьки, которые наблюдаются при кипении. Важно понимать, что в этих пузырьках находится не воздух, а именно пар, который образовывается в процессе кипения. После образования пузырьков количество пара в них растет, и они начинают увеличиваться в размерах. Зачастую, изначально пузырьки образуются вблизи стенок сосуда и не сразу поднимаются на поверхность; сначала они, увеличиваясь в размерах, оказываются под воздействием нарастающей силы Архимеда, а затем отрываются от стенки и поднимаются на поверхность, где лопаются и высвобождают порцию пара.
Стоит отметить, что далеко не сразу все пузырьки пара достигают свободной поверхности воды. В начале процесса кипения вода прогрета еще далеко не равномерно и нижние слои, вблизи которых происходит непосредственно процесс теплопередачи, еще горячее верхних, даже с учетом процесса конвекции. Это приводит к тому, что поднимающиеся снизу пузырьки пара схлопываются из-за явления поверхностного натяжения, еще не доходя до свободной поверхности воды. При этом пар, который находился внутри пузырьков, переходит в воду, тем самым дополнительно нагревая ее и ускоряя процесс равномерного прогрева воды по всему объему. В результате, когда вода прогревается практически равномерно, почти все пузырьки пара начинают достигать поверхности воды и начинается процесс интенсивного парообразования.
Важно выделить тот факт, что температура, при которой проходит процесс кипения, остается неизменной даже в том случае, если увеличивать интенсивность подвода тепла к жидкости. Простыми словами, если в процессе кипения прибавить газ на конфорке, которая разогревает кастрюлю с водой, то это приведет только к увеличению интенсивности кипения, а не к увеличению температуры жидкости. Если углубляться более серьезно в процесс кипения, то стоит отметить, что в воде возникают области, в которых она может быть перегрета выше температуры кипения, но величина такого перегрева, как правило, не превышает одного-пары градусов и незначительна в общем объеме жидкости. Температура кипения воды при нормальном давлении составляет 100°С.
В процессе кипения воды можно заметить, что он сопровождается характерными звуками так называемого бурления. Эти звуки возникают как раз из-за описанного процесса схлопывания пузырьков пара.
Процессы кипения других жидкостей протекают аналогичным образом, что и кипение воды. Основное отличие в этих процессах составляют различные температуры кипения веществ, которые при нормальном атмосферном давлении являются уже измеренными табличными величинами. Укажем основные значения этих температур в таблице.
Интересен тот факт, что температура кипения жидкостей зависит от величины атмосферного давления, поэтому мы и указывали, что все значения в таблице приведены при нормальном атмосферном давлении. При возрастании давления воздуха возрастает и температура кипения жидкости, при уменьшении, наоборот, уменьшается.
На этой зависимости температуры кипения от давления окружающей среды основан принцип работы такого известного кухонного прибора, как скороварка (рис. 2). Она представляет собой кастрюлю с плотно закрывающейся крышкой, под которой в процессе парообразования воды давление воздуха с паром достигает значения до 2 атмосферных давлений, что приводит к увеличению температуры кипения воды в ней до . Из-за этого вода с продуктами в ней имеют возможность нагреться до температуры выше, чем обычно (), и процесс приготовления ускоряется. Из-за такого эффекта устройство и получило свое название.

Рис. 2. Скороварка ()
Ситуация с уменьшением температуры кипения жидкости с понижением атмосферного давления также имеет пример из жизни, но уже не повседневной для многих людей. Относится такой пример к путешествиям альпинистов в высокогорных районах. Оказывается, что в местности, находящейся на высоте 3000-5000 м, температура кипения воды из-за уменьшения атмосферного давления снижается до и более низких значений, что приводит к сложностям при приготовлении пищи в походах, т. к. для эффективной термической обработки продуктов в таком случае требуется значительно большее время, чем при нормальных условиях. На высотах около 7000 м температура кипения воды доходит до , что приводит к невозможности приготовления многих продуктов в таких условиях.
На том, что температуры кипения различных веществ отличаются, основаны некоторые технологии разделения веществ. Например, если рассматривать нагревание нефти, которая представляет собой сложную жидкость, состоящую из множества компонентов, то в процессе кипения ее можно будет разделить на несколько различных веществ. В данном случае, благодаря тому, что температуры кипения керосина, бензина, лигроина и мазута различны, их можно отделить друг от друга путем парообразования и конденсации при различных температурах. Такой процесс, как правило, называют разделением на фракции (рис. 3).

Рис. 3 Разделение нефти на фракции ()
Как и любой физический процесс, кипение необходимо характеризовать с помощью какой-то численной величины, такую величину называют удельной теплотой парообразования.
Для того чтобы понять физический смысл этой величины, рассмотрим следующий пример: возьмем 1 кг воды и доведем ее до температуры кипения, затем замерим, какое количество теплоты необходимо для того, чтобы полностью испарить эту воду (без учета тепловых потерь) - эта величина и будет равна удельной теплоте парообразования воды. Для другого вещества это значение теплоты будет другим и будет являться удельной теплотой парообразования этого вещества.
Удельная теплота парообразования оказывается очень важной характеристикой в современных технологиях производства металлов. Оказывается, что, например, при плавлении и испарении железа с его последующей конденсацией и затвердеванием образуется кристаллическая решетка с такой структурой, которая обеспечивает более высокую прочность, чем исходный образец.
Обозначение : удельная теплота парообразования и конденсации (иногда обозначается ).
Единица измерения : .
Удельная теплота парообразования веществ определяется с помощью экспериментов в лабораторных условиях, и ее значения для основных веществ занесены в соответствующую таблицу.
|
Вещество |
Из §§ 2.5 и 7.2 следует, что при парообразовании внутренняя энергия вещества увеличивается, а при конденсации - уменьшается. Поскольку при этих процессах температуры жидкости и ее пара могут быть равными, изменение внутренней энергии вещества происходит только за счет изменения потенциальной энергии молекул. Итак, при одной и той же температуре единица массы жидкости имеет меньшую внутреннюю энергию, чем единица массы ее пара.
Опыт показывает, что плотность вещества в процессе парообразования сильно уменьшается, а объем, занятый веществом, увеличивается. Следовательно, при парообразовании должна совершаться работа против сил внешнего давления. Поэтому энергия, которую нужно сообщить жидкости для превращения ее в пар при неизменной температуре, частично идет на увеличение внутренней энергии вещества и частично - на выполнение работы против внешних сил в процессе его расширения.
На практике для превращения жидкости в пар в процессе теплообмена к ней подводится теплота. Количество теплоты необходимое для превращения жидкости в пар при неизменной температуре, называется теплотой парообразования. При превращении пара в жидкость от него необходимо отвести количество теплоты которое называют теплотой конденсации. Если внешние условия одинаковы, то при равных массах одинакового вещества теплота парообразования равна теплоте конденсации.
С помощью калориметра было установлено, что теплота парообразования прямо пропорциональна превращенной в пар массе жидкости
Здесь - коэффициент пропорциональности, величина которого зависит от рода жидкости и внешних условий.
Величина которая характеризует зависимость теплоты парообразования от рода вещества и от внешних условий, называется удельной теплотой парообразования. Удельная теплота парообразования измеряется количеством теплоты, необходимым для превращения в пар единицы массы жидкости при неизменной температуре:
В СИ за единицу принимают удельную теплоту парообразования такой жидкости, для превращения в пар 1 кг которой при неизменной температуре требуется 1 Дж теплоты. (Покажите это с помощью формулы (7.1а).)
В качестве примера отметим, что удельная теплота парообразования воды при температуре (100°С) равна
Поскольку парообразование может происходить при различных температурах, возникает вопрос: будет ли при этом изменяться удельная теплота парообразования вещества? Опыт показывает, что при повышении температуры удельная теплота парообразования уменьшается. Происходит это потому, что все жидкости при нагревании расширяются. Расстояние между молекулами при этом возрастает и силы молекулярного взаимодействия уменьшаются. Кроме того, чем выше температура, тем больше среднее значение энергии У молекул жидкости и тем меньше энергии им нужно добавить, чтобы они могли вылететь за пределы поверхности жидкости.